Ш§Щ„Щ…ЩӮШҜЩ…Ш©
Ш§Щ„Щ…Ш§ШҜШ© ЩҒЩҠ Ш§Щ„ЩҲШіШ· Ш§Щ„Щ…ШӯЩҠШ·
Ш§Щ„Щ…ЩҲШ§ШҜ Ш§Щ„ЩғЩҠЩ…ЩҠШ§ШҰЩҠШ© Ш§Щ„ЩҶЩӮЩҠШ© ЩҒЩҠ Ш§Щ„ЩҲШіШ· Ш§Щ„Щ…ШӯЩҠШ·
Ш§Щ„Ш°ШұШ§ШӘ ЩҲШ§Щ„Ш¬ШІЩҠШҰШ§ШӘ
ШЁЩҶЩҠШ© Ш§Щ„Ш°ШұШ©
Ш§Щ„ШӘЩҒШ§Ш№Щ„Ш§ШӘ ЩҲШ§Щ„ШӘЩҲШ§ШІЩҶ
Ш§Щ„Ш§ШіШі ЩҲ Ш§Щ„Ш§ШӯЩ…Ш§Ш¶
Ш§Щ„Щ…Ш№Ш§ШҜЩҶ ЩҲШ§Щ„Ш§Щ…Ш№Ш§ШҜЩҶ
Ш§Щ„Щ…Ш№Ш§ШҜЩҶ ЩҲШ§Щ„Ш§Щ…Ш№Ш§ШҜЩҶ 2
Ш§Щ„ЩғШұШЁЩҲЩҶ ЩҲЩ…ШұЩғШЁШ§ШӘЩҮ
Ш§Щ„Ш¬ШҜЩҲЩ„ Ш§Щ„ШҜЩҲШұЩҠ Щ„Щ„Ш№ЩҶШ§ШөШұ
Ш§Щ„Ш§Щ„ЩҠШ§ЩҒ Ш§Щ„ШөЩҶШ§Ш№ЩҠШ© ЩҲШ§Щ„ШЁЩ„Ш§ШіШӘЩҠЩғ
Ш§Щ„ЩҒШӯЩ… ЩҲШ§Щ„ШЁШӘШұЩҲЩ„
Ш§Щ„Ш§ШӯШӘШұШ§ЩӮ ЩҲШ§Щ„Щ„ЩҮШЁ
ЩҠЩ„Ш№ШЁ Ш§Щ„ЩғШұШЁЩҲЩҶ ШҜЩҲШұШ§ЩӢ Щ…ЩҮЩ…Ш§ЩӢ Ш¬ШҜЩӢШ§ ЩҒЩҠ ШӯЩҠШ§Ш© Ш¬Щ…ЩҠШ№ Ш§Щ„ЩғШ§ШҰЩҶШ§ШӘ Ш§Щ„ШӯЩҠШ©.
ШӘШЁЩ„Шә ЩҶШіШЁШ© Ш§Щ„ЩғШұШЁЩҲЩҶ ЩҒЩҠ Ш§Щ„ЩӮШҙШұШ© Ш§Щ„ШЈШұШ¶ЩҠШ© 0.02ЩӘ ЩҒЩӮШ· ШҢ ЩҲЩҮЩҲ Щ…ШӘЩҲЩҒШұ ЩҒЩҠ ШҙЩғЩ„ Щ…Ш№Ш§ШҜЩҶ Щ…Ш«Щ„ Ш§Щ„ЩғШұШЁЩҲЩҶШ§ШӘ ЩҲЩғШұШЁЩҲЩҶШ§ШӘ Ш§Щ„ЩҮЩҠШҜШұЩҲШ¬ЩҠЩҶ ЩҲШ§Щ„ЩҒШӯЩ… ЩҲШ§Щ„ЩҶЩҒШ·.
ЩҶШіШЁШ© ЩҲШ¬ЩҲШҜ Ш§Щ„ЩғШұШЁЩҲЩҶ ЩҒЩҠ Ш§Щ„ШәЩ„Ш§ЩҒ Ш§Щ„Ш¬ЩҲЩҠ Щ„Щ„ШЈШұШ¶ 0.03ЩӘ ШҢЩҲЩҠЩғЩҲЩҶ Ш№Щ„Щү ШҙЩғЩ„ Ш«Ш§ЩҶЩҠ ШЈЩғШіЩҠШҜ Ш§Щ„ЩғШұШЁЩҲЩҶ.
Щ…ШұЩғШЁШ§ШӘ Ш§Щ„ЩғШұШЁЩҲЩҶ
Ш¬Щ…ЩҠШ№ Щ…ШұЩғШЁШ§ШӘ Ш§Щ„ЩғШұШЁЩҲЩҶ ШӘЩӮШұЩҠШЁЩӢШ§ (ШЁШ§ШіШӘШ«ЩҶШ§ШЎ Ш§Щ„ЩӮЩ„ЩҠЩ„ Щ…ЩҶЩҮШ§) ЩҮЩҠ Щ…ЩҲШөЩҗЩ„Ш§ШӘ ШұШҜЩҠШҰШ© Щ„Щ„ЩғЩҮШұШЁШ§ШЎ.
ЩҠШӘЩғЩҲЩҶ Ш§Щ„Ш§Щ„Щ…Ш§Ші ЩҲШ§Щ„Ш¬ШұШ§ЩҒЩҠШӘ Щ…ЩҶ Ш°ШұШ§ШӘ Ш§Щ„ЩғШұШЁЩҲЩҶ. ЩҲЩ…Ш№ Ш°Щ„Щғ ШҢ ЩҠЩғЩ…ЩҶ Ш§Щ„Ш§Ш®ШӘЩ„Ш§ЩҒ ШЁЩҠЩҶЩҮЩ…Ш§ ЩҒЩҠ Ш§Щ„Ш·ШұЩҠЩӮШ© Ш§Щ„ШӘЩҠ ШӘШұШӘШЁШ· ШЁЩҮШ§ Ш°ШұШ§ШӘ Ш§Щ„ЩғШұШЁЩҲЩҶ ШЁШЁШ№Ш¶ЩҮШ§ Ш§Щ„ШЁШ№Ш¶.
ЩҒЩҠ Ш§Щ„Ш§Щ„Щ…Ш§Ші ШҢ ШӘШұШӘШЁШ· ЩғЩ„ Ш°ШұШ© Щ…ЩҶ Ш§Щ„ЩғШұШЁЩҲЩҶ ШЁШЈШұШЁШ№ Ш°ШұШ§ШӘ ЩғШұШЁЩҲЩҶ ШЈШ®ШұЩү ЩҲШӘШҙЩғЩ„ ШЁЩҶЩҠШ© ШөЩ„ШЁШ© Ш«Щ„Ш§Ш«ЩҠШ© Ш§Щ„ШЈШЁШ№Ш§ШҜ (Ш§ЩҶШёШұ Ш§Щ„ШөЩҲШұШ© ШЈШҜЩҶШ§ЩҮ).
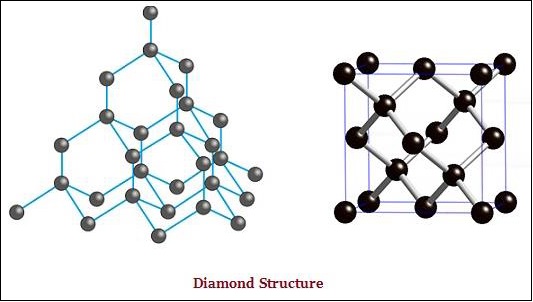
ЩҒЩҠ Ш§Щ„Ш¬ШұШ§ЩҒЩҠШӘ ШҢ ЩғЩ„ Ш°ШұШ© Щ…ЩҶ Ш§Щ„ЩғШұШЁЩҲЩҶ Щ…ШұШӘШЁШ·Ш© ШЁШ«Щ„Ш§Ш« Ш°ШұШ§ШӘ ЩғШұШЁЩҲЩҶ ШЈШ®ШұЩү ЩҒЩҠ ЩҶЩҒШі Ш§Щ„Щ…ШіШӘЩҲЩү ШҢ Щ…Щ…Ш§ ЩҠШ№Ш·ЩҠ ШҙЩғЩ„ Щ…ШөЩҒЩҲЩҒШ© ШіШҜШ§ШіЩҠШ© (Ш§ЩҶШёШұ Ш§Щ„ШөЩҲШұШ© ШЈШҜЩҶШ§ЩҮ) :
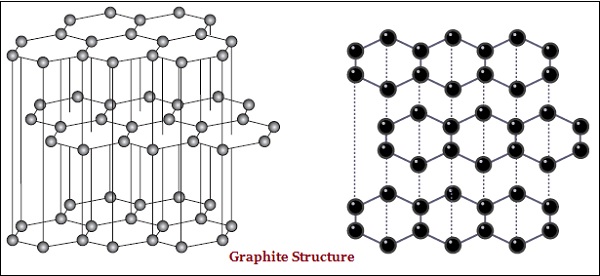
ЩҮЩҶШ§Щғ ШЈЩҠШ¶ЩӢШ§ Ш§Ш®ШӘЩ„Ш§ЩҒ ЩҒЩҠ ШЁШ№Ш¶ Ш§Щ„ШЁЩҶЩҠШ§ШӘ Ш§Щ„ЩҒЩҠШІЩҠШ§ШҰЩҠШ© Щ„Щ„ШЈЩ„Щ…Ш§Ші ЩҲШ§Щ„Ш¬ШұШ§ЩҒЩҠШӘ.
Ш§Щ„Ш§Щ„Щ…Ш§Ші ЩҮЩҲ ШЈЩӮШіЩү Щ…Ш§ШҜШ© Щ…Ш№ШұЩҲЩҒШ© ШЁЩҠЩҶЩ…Ш§ Ш§Щ„Ш¬ШұШ§ЩҒЩҠШӘ Щ…Ш§ШҜШ© ЩҶШ§Ш№Щ…Ш© ЩҲШІЩ„ЩӮШ©.
Ш§Щ„Ш¬ШұШ§ЩҒЩҠШӘ Щ…ЩҲШөЩҗЩ„ Ш¬ЩҠШҜ Щ„Щ„ЩғЩҮШұШЁШ§ШЎ ШЁЩҠЩҶЩ…Ш§ Ш§Щ„Ш§Щ„Щ…Ш§Ші Щ„ЩҠШі ЩғШ°Щ„Щғ.
ЩҠЩҲШ¶Шӯ Ш§Щ„Ш¬ШҜЩҲЩ„ Ш§Щ„ШӘШ§Щ„ЩҠ ШЁЩҶЩҠШ§ШӘ Щ…ШұЩғШЁШ§ШӘ Ш§Щ„ЩғШұШЁЩҲЩҶ ЩҲШ§Щ„ЩҮЩҠШҜШұЩҲШ¬ЩҠЩҶ
|
Ш§ШіЩ… Ш§Щ„Щ…ШұЩғШЁ |
ШөЩҠШәШ© Ш§Щ„Щ…ШұЩғШЁ |
Ш§Щ„ШЁЩҶЩҠШ© |
|
Methane Щ…ЩҠШ«Ш§ЩҶ |
CH4 |
 |
|
Ethane Ш§ЩҠШ«Ш§ЩҶ |
C2H6 |
 |
|
Propane ШЁШұЩҲШЁШ§ЩҶ |
C3H8 |
 |
|
Butane ШЁЩҲШӘШ§ЩҶ |
C4H10 |
 |
|
Pentane ШЁЩҶШӘШ§ЩҶ |
C5H12 |
 |
|
Hexane ЩҮЩғШіШ§ЩҶ |
C6H14 |
 |
ШӘЩҸШ№ШұЩҒ Ш§Щ„Щ…ШұЩғШЁШ§ШӘ ШҢ Ш§Щ„ШӘЩҠ Щ„ЩҮШ§ ШӘШұЩғЩҠШЁШ© Ш¬ШІЩҠШҰЩҠШ© Щ…ШӘШ·Ш§ШЁЩӮШ© ШҢ ЩҲЩ„ЩғЩҶ Щ„ЩҮШ§ ШЁЩҶЩҠШ© Щ…Ш®ШӘЩ„ЩҒШ© ШҢ ШЁШ§ШіЩ… ШЈЩҠШІЩҲЩ…ШұШ§ШӘ ЩҮЩҠЩғЩ„ЩҠШ© (Ш§ЩҶШёШұ ШЁЩҶЩҠШ© Ш§Щ„ШЁЩҠЩҲШӘШ§ЩҶ Ш§Щ„ЩҲШ§ШұШҜШ© ШЈШҜЩҶШ§ЩҮ).
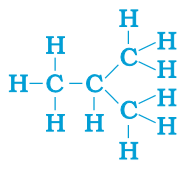
ШӘЩҸШ№ШұЩҒ Ш§Щ„ЩҮЩҠШҜШұЩҲЩғШұШЁЩҲЩҶШ§ШӘ Ш§Щ„Щ…ШҙШЁШ№Ш© ШЁШ§Щ„ШЈЩ„ЩғШ§ЩҶШ§ШӘ.
ШӘЩҸШ№ШұЩҒ Ш§Щ„ЩҮЩҠШҜШұЩҲЩғШұШЁЩҲЩҶШ§ШӘ ШәЩҠШұ Ш§Щ„Щ…ШҙШЁШ№Ш© ШҢ Ш§Щ„ШӘЩҠ ШӘШӘЩғЩҲЩҶ Щ…ЩҶ ШұШ§ШЁШ·Ш© Щ…ШІШҜЩҲШ¬Ш© ЩҲШ§ШӯШҜШ© ШЈЩҲ ШЈЩғШ«Шұ ШҢ ШЁШ§Щ„ШЈЩ„ЩғЩҠЩҶШ§ШӘ.
ШӘЩҸШ№ШұЩҒ Ш§Щ„ЩҮЩҠШҜШұЩҲЩғШұШЁЩҲЩҶШ§ШӘ ШәЩҠШұ Ш§Щ„Щ…ШҙШЁШ№Ш© ШҢ ЩҲШ§Щ„ШӘЩҠ ШӘШӘЩғЩҲЩҶ Щ…ЩҶ ЩҲШ§ШӯШҜ ШЈЩҲ ШЈЩғШ«Шұ Щ…ЩҶ Ш§Щ„ШұЩҲШ§ШЁШ· Ш§Щ„Ш«Щ„Ш§Ш«ЩҠШ© ШҢ ШЁШ§ШіЩ… Ш§Щ„ШЈЩ„ЩғЩҠЩҶШ§ШӘ.
Ш§ШіШӘШ®ШҜШ§Щ… Ш§Щ„ЩғШӯЩҲЩ„ЩҠШ§ШӘ ЩғЩҲЩӮЩҲШҜ
ШӘШ№Щ…Щ„ ЩҶШЁШ§ШӘШ§ШӘ ЩӮШөШЁ Ш§Щ„ШіЩғШұ ШЁЩғЩҒШ§ШЎШ© Ш№Ш§Щ„ЩҠШ© Ш№Щ„Щү ШӘШӯЩҲЩҠЩ„ Ш¶ЩҲШЎ Ш§Щ„ШҙЩ…Ші ШҘЩ„Щү Ш·Ш§ЩӮШ© ЩғЩҠЩ…ЩҠШ§ШҰЩҠШ© ЩҲЩҠЩ…ЩғЩҶ Ш§ШіШӘШ®ШҜШ§Щ… Ш№ШөЩҠШұЩҮ ЩҒЩҠ ШӘШӯШ¶ЩҠШұ ШҜШЁШі Ш§Щ„ШіЩғШұ.
Ш№ЩҶШҜЩ…Ш§ ЩҠШӘШ®Щ…Шұ ШҜШЁШі Ш§Щ„ШіЩғШұ ШҢ ЩҒШҘЩҶЩҮ ЩҠЩҶШӘШ¬ Ш§Щ„ЩғШӯЩҲЩ„ (Ш§Щ„ШҘЩҠШ«Ш§ЩҶЩҲЩ„).
ШӘШіШӘШ®ШҜЩ… ШЁШ№Ш¶ Ш§Щ„ШҜЩҲЩ„ Ш§Щ„ШўЩҶ Ш§Щ„ЩғШӯЩҲЩ„ ЩғЩ…Ш§ШҜШ© Щ…Ш¶Ш§ЩҒШ© Щ„Щ„ШЁЩҶШІЩҠЩҶ ШҢ ШӯЩҠШ« ШЈЩҶЩҮ ЩҲЩӮЩҲШҜ ШЈЩҶШёЩҒ.
ЩҮШ°ЩҮ Ш§Щ„ЩғШӯЩҲЩ„ ШҢ Ш№ЩҶШҜ Ш§ШӯШӘШұШ§ЩӮЩҮШ§ ЩҒЩҠ ЩҮЩҲШ§ШЎ ЩғШ§ЩҒЩҚ (ШЈЩғШіШ¬ЩҠЩҶ) ШҢ ЩҠЩҶШӘШ¬ Ш№ЩҶЩҮШ§ Ш«Ш§ЩҶЩҠ ШЈЩғШіЩҠШҜ Ш§Щ„ЩғШұШЁЩҲЩҶ ЩҲШ§Щ„Щ…Ш§ШЎ ЩҒЩӮШ·.
Ш§Щ„Ш§ШіШӘШұШ§ШӘ
Ш§Щ„ШҘШіШӘШұШ§ШӘ ЩҮЩҠ Щ…ЩҲШ§ШҜ Ш°Ш§ШӘ ШұШ§ШҰШӯШ© ШӯЩ„ЩҲШ© ШҢ ЩҲШ§Щ„ШӘЩҠ ШӘШӘШҙЩғЩ„ ШЁШҙЩғЩ„ ШәШ§Щ„ШЁШ§ЩӢ Ш№ЩҶ Ш·ШұЩҠЩӮ ШӘЩҒШ§Ш№Щ„ ШӯЩ…Ш¶ ЩҲЩғШӯЩҲЩ„ (Ш§ЩҶШёШұ Ш§Щ„ШөЩҲШұШ© ШЈШҜЩҶШ§ЩҮ - ШӘЩҲШ¶Шӯ ШӘЩғЩҲЩҠЩҶ Ш§Щ„ШҘШіШӘШұШ§ШӘ).
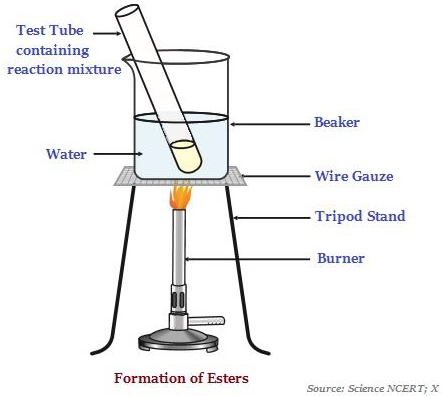
Ш№ЩҶШҜЩ…Ш§ ШӘШӘЩҒШ§Ш№Щ„ Ш§Щ„ШҘШіШӘШұШ§ШӘ ЩҒЩҠ ЩҲШ¬ЩҲШҜ ШӯЩ…Ш¶ ШЈЩҲ Ш§ШіШ§ШіШҢ ЩҒШҘЩҶЩҮШ§ ШӘШұШ¬Ш№ Ш§Щ„ЩғШӯЩҲЩ„ ЩҲШӯЩ…Ш¶ Ш§Щ„ЩғШұШЁЩҲЩғШіЩҠЩ„.
ЩҠЩҸШ№ШұЩҒ ШӘЩҒШ§Ш№Щ„ Ш§Щ„ШҘШіШӘШұШ§ШӘ Щ…Ш№ ШӯЩ…Ш¶ ШЈЩҲ ЩӮШ§Ш№ШҜШ© ШЁШ№Щ…Щ„ЩҠШ© Ш§Щ„ШӘШөШЁЩҶ Щ„ШЈЩҶЩҮ ЩҠШіШӘШ®ШҜЩ… ЩҒЩҠ ШӘШӯШ¶ЩҠШұ Ш§Щ„ШөШ§ШЁЩҲЩҶ.
Ш№Ш§ШҜШ©ЩӢ Щ…Ш§ ШӘЩғЩҲЩҶ Ш¬ШІЩҠШҰШ§ШӘ Ш§Щ„ШөШ§ШЁЩҲЩҶ Ш№ШЁШ§ШұШ© Ш№ЩҶ ШЈЩ…Щ„Ш§Шӯ Ш§Щ„ШөЩҲШҜЩҠЩҲЩ… ШЈЩҲ Ш§Щ„ШЁЩҲШӘШ§ШіЩҠЩҲЩ… Щ…ЩҶ Ш§Щ„ШЈШӯЩ…Ш§Ш¶ Ш§Щ„ЩғШұШЁЩҲЩғШіЩҠЩ„ЩҠШ© Ш·ЩҲЩҠЩ„Ш© Ш§Щ„ШіЩ„ШіЩ„Ш©.
ЩҲЩ…ЩҶ Ш§Щ„Щ…Ш«ЩҠШұ Щ„Щ„Ш§ЩҮШӘЩ…Ш§Щ… ШЈЩҶ Ш§Щ„Ш·ШұЩҒ Ш§Щ„ШЈЩҠЩҲЩҶЩҠ Щ„Щ„ШөШ§ШЁЩҲЩҶ ЩҠШ°ЩҲШЁ ЩҒЩҠ Ш§Щ„Щ…Ш§ШЎ ШЁЩҠЩҶЩ…Ш§ ШӘШ°ЩҲШЁ ШіЩ„ШіЩ„Ш© Ш§Щ„ЩғШұШЁЩҲЩҶ ЩҒЩҠ Ш§Щ„ШІЩҠШӘ. ШӘШҙЩғЩ„ ЩҮШ°ЩҮ Ш§Щ„Щ…ЩҠШІШ§ШӘ Ш§Щ„ЩҶЩ…ЩҲШ°Ш¬ЩҠШ© Щ„Ш¬ШІЩҠШҰШ§ШӘ Ш§Щ„ШөШ§ШЁЩҲЩҶ ШЁЩҶЩү ШӘШ№ШұЩҒ ШЁШ§ШіЩ… Ш§Щ„Щ…Ш°ЩҠЩ„Ш§ШӘ (Ш§ЩҶШёШұ Ш§Щ„ШөЩҲШұШ© ШЈШҜЩҶШ§ЩҮ)
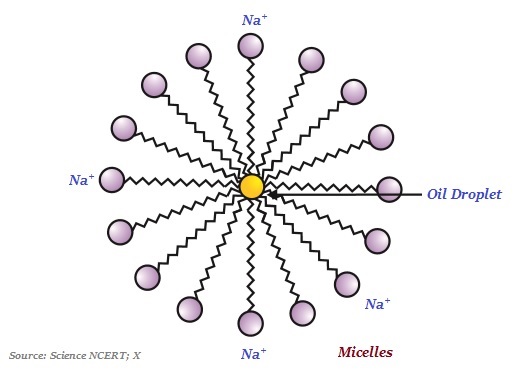
ЩҒЩҠ Ш§Щ„ШЈЩҠЩҲЩҶ Ш§Щ„ШәШұЩҲЩҠ micelles ШҢ ЩҠЩғЩҲЩҶ ШЈШӯШҜ Ш·ШұЩҒЩҠ Ш§Щ„Ш¬ШІЩҠШҰШ§ШӘ ШЁШ§ШӘШ¬Ш§ЩҮ ЩӮШ·ШұШ© Ш§Щ„ШІЩҠШӘ ШЁЩҠЩҶЩ…Ш§ ШӘШёЩ„ Ш§Щ„ЩҶЩҮШ§ЩҠШ© Ш§Щ„ШЈЩҠЩҲЩҶЩҠШ© ЩҒЩҠ Ш§Щ„Ш®Ш§ШұШ¬.
ЩҠШіШ§Ш№ШҜ Ш§Щ„ШЈЩҠЩҲЩҶ Ш§Щ„ШәШұЩҲЩҠ micelles Ш§Щ„ШөШ§ШЁЩҲЩҶ ЩҒЩҠ ШҘШ°Ш§ШЁШ© Ш§Щ„ШЈЩҲШіШ§Ш® ЩҒЩҠ Ш§Щ„Щ…Ш§ШЎ Шӣ ЩҲШЁШ§Щ„Щ…Ш«Щ„ ШҢ ЩҠШӘЩ… ШӘЩҶШёЩҠЩҒ Ш§Щ„Щ…Щ„Ш§ШЁШі.
Щ…ЩҶ ЩҶШ§ШӯЩҠШ© ШЈШ®ШұЩү ШҢ Ш§Щ„Щ…ЩҶШёЩҒШ§ШӘ Ш№Ш§ШҜШ© Щ…Ш§ ШӘЩғЩҲЩҶ ШЈЩ…Щ„Ш§Шӯ Ш§Щ„ШЈЩ…ЩҲЩҶЩҠЩҲЩ… ШЈЩҲ Ш§Щ„ШіЩ„ЩҒЩҲЩҶШ§ШӘ Щ…ЩҶ Ш§Щ„ШЈШӯЩ…Ш§Ш¶ Ш§Щ„ЩғШұШЁЩҲЩғШіЩҠЩ„ЩҠШ© Ш·ЩҲЩҠЩ„Ш© Ш§Щ„ШіЩ„ШіЩ„Ш© ШҢ ЩҲШ§Щ„ШӘЩҠ ШӘШёЩ„ ЩҒШ№Ш§Щ„Ш© ШӯШӘЩү ЩҒЩҠ Ш§Щ„Щ…Ш§ШЎ Ш§Щ„Ш№ШіШұ.
ШӘЩҸШіШӘШ®ШҜЩ… Ш§Щ„Щ…ЩҶШёЩҒШ§ШӘ Ш№Ш§ШҜШ©ЩӢ ЩҒЩҠ ШөЩҶШ№ Ш§Щ„ШҙШ§Щ…ШЁЩҲ ЩҲШЁШ№Ш¶ Ш§Щ„Щ…ЩҶШӘШ¬Ш§ШӘ Ш§Щ„ШЈШ®ШұЩү Щ„ШӘЩҶШёЩҠЩҒ Ш§Щ„Щ…Щ„Ш§ШЁШі.
Щ„Ш§ ЩҠЩҲШ¬ШҜ ШӘШ№Щ„ЩҠЩӮШ§ШӘ
Щ„Ш§Ш¶Ш§ЩҒШ© ШіШӨШ§Щ„ Ш§ЩҲ ШӘШ№Щ„ЩҠЩӮ Ш№Щ„Щү Ш§Щ„ШҜШұШі ЩҠШӘЩҲШ¬ШЁ Ш№Щ„ЩҠЩғ ШӘШіШ¬ЩҠЩ„ Ш§Щ„ШҜШ®ЩҲЩ„
ШӘШіШ¬ЩҠЩ„ Ш§Щ„ШҜШ®ЩҲЩ„